¤o(w©▓)ÖC(j©®)ŠÅ╬g䮥─ū„ė├ÖC(j©®)└Ē
į┌ļŖĮŌ┘|(zh©¼)╚▄ę║ųąŻ¼Įī┘Ą─Ė»╬g▀^(gu©░)│╠Ę■Å─ļŖ╗»īW(xu©”)▀^(gu©░)│╠Ż¼ę“┤╦Ė»╬gĄ─░l(f©Ī)╔·┤µį┌ų°ĻÄśOĘ┤æ¬(y©®ng)┼cĻ¢(y©óng)śOĘ┤æ¬(y©®ng)ĪŻĻÄśOĘ┤æ¬(y©®ng)ī”(du©¼)æ¬(y©®ng)Ą─╩Ū╚źśO╗»ä®Įė╩▄ļŖūėĄ─▀^(gu©░)│╠Ż¼ūŅ│ŻęŖ(ji©żn)Ą─ā╔ĘN╚źśO╗»ä®×ķÜõ┘|(zh©¼)ūė┼cč§ÜŌŻ¼Č°Ļ¢(y©óng)śOĘ┤æ¬(y©®ng)ī”(du©¼)æ¬(y©®ng)Ą─╩ŪĮī┘Ą─╚▄ĮŌ▀^(gu©░)│╠ĪŻÅ─Ė»╬gļŖ╗»īW(xu©”)įŁ└ĒĘų╬÷Ż¼ŠÅ╬gä®╝ė╚ļ║¾╩╣Ą├Ė»╬gĘ┤æ¬(y©®ng)Ą─Ļ¢(y©óng)śO▀^(gu©░)│╠╗“š▀ĻÄśO▀^(gu©░)│╠╩▄ĄĮęųųŲŻ¼ėąą®ŠÅ╬gä®┐╔ęį═¼Ģr(sh©¬)ęųųŲĖ»╬gĘ┤æ¬(y©®ng)Ą─ĻÄśO┼cĻ¢(y©óng)śO▀^(gu©░)│╠ĪŻ
┤¾ČÓöĄ(sh©┤)¤o(w©▓)ÖC(j©®)ą═ŠÅ╬gä®ų„ę¬╩╣ė├į┌ųąąį╗“Ų½ēAąįĄ─Įķ┘|(zh©¼)Łh(hu©ón)Š│ųąŻ¼╦³éā═©│Żī”(du©¼)ļŖśOĄ─Ļ¢(y©óng)śO▀^(gu©░)│╠ėą’@ų°Ą─ęųųŲū„ė├Ż¼═©▀^(gu©░)╩╣Įī┘▒Ē├µŌg╗»╗“š▀į┌Įī┘▒Ē├µą╬│╔│┴Ęe─ż▀M(j©¼n)Č°ŲĄĮŠÅ╬gū„ė├ĪŻļSų°ŠÅ╬gä®æ¬(y©®ng)ė├Ą─░l(f©Ī)š╣Ż¼¤o(w©▓)ÖC(j©®)ŠÅ╬g䮥─╩╣ė├▓ó╬┤ŠųŽ▐į┌ųąąį╗“ēAąįĮķ┘|(zh©¼)ųąŻ¼╚ńį┌╦ßąįĮķ┘|(zh©¼)ųą╠Ē╝ėĄŌ╗»╬’ĪóüåŃ~ĪóüåõR¹}║¾Ż¼─▄’@ų°į÷ÅŖ(qi©óng)ėąÖC(j©®)ŠÅ╬g䮥─ū„ė├ą¦╣¹ĪŻėąÖC(j©®)ŠÅ╬gä®į┌╦ßąįĮķ┘|(zh©¼)ųąĄ─╩╣ė├ĘŪ│ŻÅVĘ║Ż¼╦³éā═©▀^(gu©░)╬’└Ē╗“╗»īW(xu©”)ū„ė├┴”╬³ĖĮį┌Įī┘▒Ē├µŻ¼═©▀^(gu©░)Ė─ūāļpļŖīėĮY(ji©”)śŗ(g©░u)Ż¼╠ßĖ▀Ė»╬gĘ┤æ¬(y©®ng)╗Ņ╗»─▄ęį╝░īóĖ»╬gĮķ┘|(zh©¼)┼cĮī┘╗∙¾wĖ¶ļxŻ¼▀M(j©¼n)Č°ęųųŲĖ»╬g╦┘┬╩Ż¼ėąÖC(j©®)ŠÅ╬gä®į┌ųąąįĮķ┘|(zh©¼)ųąę▓╚ĪĄ├┴╦│╔╣”Ą─æ¬(y©®ng)ė├Ż¼╚ńėąÖC(j©®)┴ū╦ß¹}Īó▒ĮŌø╦ß¹}Īó▀õ▀“▀°į┌╣żśI(y©©)╦«║═ė═╠’╬█╦«╠Ä└ĒĄ─æ¬(y©®ng)ė├ĪŻ
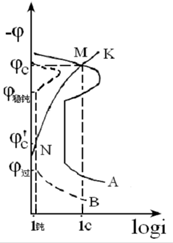
╔ŽłD×ķĻ¢(y©óng)śOęųųŲą═Ōg╗»ä®ū„ė├įŁ└ĒłDŻ¼«ö(d©Īng)Įķ┘|(zh©¼)ųą┤µį┌Ļ¢(y©óng)śOęųųŲą═ŠÅ╬gä®Ģr(sh©¬)Ż¼śO╗»Ū·ŠĆĻ¢(y©óng)śO▓┐ĘųÅ─╗Ņ╗»ģ^(q©▒)▐D(zhu©Żn)×ķŌg╗»ģ^(q©▒)Ż¼╩╣Ą├Ė»╬gļŖ┴„├▄Č╚’@ų°ĮĄĄ═Ż¼Č°śO╗»Ū·ŠĆĄ─ĻÄśO▓┐Ęų▓óø](m©”i)ėą’@ų°Ą─Ė─ūāĪŻ
(2)ĻÄśOą═ŠÅ╬gä®
Įķ┘|(zh©¼)ųąėąĻÄśOą═ŠÅ╬gä®┤µį┌Ģr(sh©¬)Ż¼śO╗»Ū·ŠĆĄ─ĻÄśO▓┐Ęų╦■ĘŲĀ¢ą▒┬╩├„’@į÷╝ėŻ¼Č°Ļ¢(y©óng)śO▓┐Ęų╦■ĘŲĀ¢ą▒┬╩ģsø](m©”i)ėąĖ─ūāŻ¼▀@šf(shu©Ł)├„ĻÄśOą═ŠÅ╬gä®ų„ę¬į÷╝ė┴╦ļŖśOĄ─ĻÄśOśO╗»▀^(gu©░)│╠Ż¼▀@╩╣Ą├Įī┘Ą─ķ_(k©Īi)┬ĘļŖ╬╗ęį╝░Ė»╬gļŖ┴„├▄Č╚Š∙Ž┬ĮĄĪŻĻÄśOą═ŠÅ╬gä®┐╔ęį═©▀^(gu©░)į┌Įī┘▒Ē├µĄ─ĻÄśOģ^(q©▒)│╔─żüĒ(l©ói)į÷╝ėĻÄśOśO╗»▀^(gu©░)│╠Ż¼ę▓┐╔ęį═©▀^(gu©░)╠ßĖ▀ĻÄśOĘ┤æ¬(y©®ng)Ą─▀^(gu©░)ļŖ╬╗Å─Č°ęųųŲĻÄśOĘ┤æ¬(y©®ng)Ż¼Č°į┌ųąąįĮķ┘|(zh©¼)ųąŻ¼ĻÄśO▀^(gu©░)│╠ų„ę¬×ķč§╚źśO╗»▀^(gu©░)│╠×ķŻ¼ę“┤╦ę▓┐╔ęį═©▀^(gu©░)╬³╩š¾wŽĄųąĄ─č§üĒ(l©ói)į÷╝ėĻÄśOĘ┤æ¬(y©®ng)Ą─śO╗»Ż¼Ė∙ō■(j©┤)ĻÄśOą═ŠÅ╬g䮥─▓╗═¼ū„ė├įŁ└ĒŻ¼Ųõ┐╔ęį▀M(j©¼n)ę╗▓Į╝Ü(x©¼)Ęų×ķęįŽ┬ÄūĘNŻ║
A.│╔─żŅÉ(l©©i)ĻÄśOą═ŠÅ╬gä®ĪŻ▀@ŅÉ(l©©i)ĻÄśOŠÅ╬gä®═©▀^(gu©░)┼cĮķ┘|(zh©¼)ųąĄ─╬’┘|(zh©¼)Ę┤æ¬(y©®ng)╗“š▀ūį╔Ē╬³ĖĮŻ¼į┌Įī┘Ą─ĻÄśOģ^(q©▒)ķg│╔─żŻ¼ą╬│╔Ą──ż─▄ėąą¦ĄžęųųŲĻÄśO╚źśO╗»ä®╚ńO2ĪóH+Ą╚Ž“Įń├µöU(ku©░)╔óŻ¼╩╣Ą├ĻÄśO╚źśO╗»ū„ė├╩▄ĄĮėąą¦ęųųŲŻ¼▀M(j©¼n)Č°£pŠÅ┴╦Ė»╬g╦┘┬╩ĪŻ
B.╠ßĖ▀ĻÄśOĘ┤æ¬(y©®ng)▀^(gu©░)ļŖ╬╗ŠÅ╬gä®ĪŻĖ»╬gĘ┤æ¬(y©®ng)Ą─ĻÄśO▀^(gu©░)│╠┤¾ČÓ×ķÜõ┘|(zh©¼)ūė╗“觥─▀ĆįŁĘ┤æ¬(y©®ng)Ż¼▀@ą®ĻÄśOĘ┤æ¬(y©®ng)░l(f©Ī)╔·Ą─ļŖ╬╗Š∙Ė▀ė┌Ųõ└ĒšōĄ─ŲĮ║ŌļŖ╬╗Ż¼╝┤┤µį┌▀^(gu©░)ļŖ╬╗ĪŻ╠žäe╩Ūį┌╦ßąįĮķ┘|(zh©¼)ųąŻ¼Üõ┘|(zh©¼)ūėĄ─▀ĆįŁĘ┤æ¬(y©®ng)į┌▓╗═¼Įī┘╔Ž┤µį┌’@ų°Ą─▓Ņ«ÉŻ¼Č°«ö(d©Īng)Įķ┘|(zh©¼)ųą┤µį┌ŃGĪó╣»ĪóõRĄ╚ųžĮī┘ļxūėĢr(sh©¬)Ż¼īóĢ■(hu©¼)’@ų°╠ßĖ▀Üõ┘|(zh©¼)ūėĄ─▀ĆįŁ▀^(gu©░)ļŖ╬╗Ż¼Å─Č°╩╣ĻÄśO▀^(gu©░)│╠╩▄ĄĮęųųŲŻ¼ĮĄĄ═Ė»╬gĘ┤æ¬(y©®ng)╦┘Č╚ĪŻ
C.║─觹═ĻÄśOŠÅ╬gä®ĪŻį┌ųąąįĮķ┘|(zh©¼)ųąŻ¼Ė»╬gĘ┤æ¬(y©®ng)Ą─ĻÄśO▀^(gu©░)│╠ČÓ×ķč§╚źśO╗»▀^(gu©░)│╠Ż¼ę“┤╦į┌Įķ┘|(zh©¼)ųą╝ė╚ļ┐╔ęį┼cč§░l(f©Ī)╔·Ę┤æ¬(y©®ng)Ą─╬’┘|(zh©¼)Ż¼ät┐╔ĮĄĄ═Įķ┘|(zh©¼)ųąĄ─č§║¼┴┐Ż¼╩╣ĻÄśOĘ┤æ¬(y©®ng)╩▄ĄĮęųųŲŻ¼▀M(j©¼n)Č°ęųųŲĖ»╬g╦┘┬╩ĪŻ
(3)╗ņ║Žą═ŠÅ╬gä®
įōŅÉ(l©©i)ą═ŠÅ╬gä®ī”(du©¼)Ė»╬gĄ─ĻÄĻ¢(y©óng)śOĘ┤æ¬(y©®ng)Š∙ėą├„’@Ą─ęųųŲū„ė├Ż¼ė╔ė┌╝ė╚ļ╗ņ║Žą═ŠÅ╬gä®║¾ļŖśOĄ─ĻÄĻ¢(y©óng)śO╦■ĘŲĀ¢ą▒┬╩═¼Ģr(sh©¬)į÷╝ėŻ¼ę“┤╦ūįĖ»╬gļŖ╬╗ø](m©”i)ėą’@ų°Ė─ūāŻ¼Ą½╩ŪĖ»╬gļŖ┴„├▄Č╚’@ų°ĮĄĄ═Ż¼╩╣Ą├Įī┘Ė»╬g╦┘Č╚╩▄ĄĮęųųŲĪŻ
|
